Insuficiência Pancreática: Etiologia e Tratamento
Insuficiência Pancreática: Etiologia e Tratamento
Cristiane Boé e Ulysses Fagundes Neto
Introdução
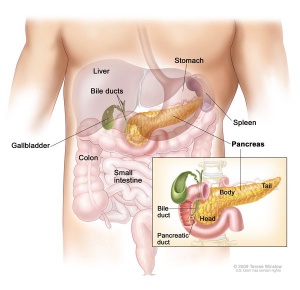
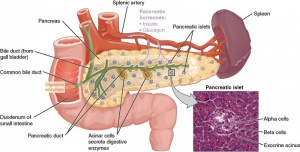
A função pancreática normal garante efetiva digestão e absorção dos nutrientes. Vale ressaltar que o pâncreas adquire plena maturidade funcional na produção enzimática a partir dos 2 anos de idade (Figuras 1-2-3).
Por outro lado, as manifestações clínicas da insuficiência pancreática (IP) ocorrem quando as secreções exócrinas do pâncreas não mantêm uma função digestiva normal, afetando a qualidade de vida e, como consequência, pode resultar em desnutrição.
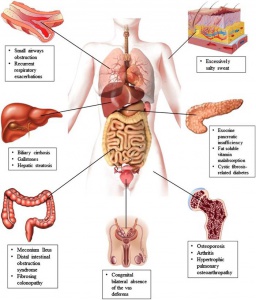
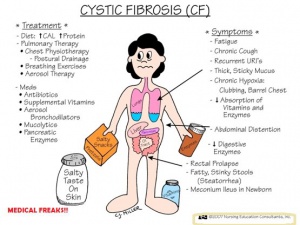
A principal causa de IP é a pancreatite crônica, que apresenta a estimativa de afetar 0,4% a 5% da população mundial. Entretanto, em crianças, a causa mais comum é a fibrose cística (FC). A prevalência de IP exócrina nos casos de pancreatite crônica é de 30 a 40%, enquanto que na FC é de 80 a 90% (Figura C).
Desde 1938, após a aprovação pelo Food and Drug Administration (FDA), a reposição de enzimas pancreáticos tem sido a principal ação terapêutica para aqueles pacientes que sofrem de má absorção dos nutrientes secundária à insuficiência pancreática. O nível das enzimas pancreáticas secretadas no intestino delgado varia segundo a quantidade e o tipo de lipídios ingeridos durante uma refeição, além de também apresentar uma oscilação individual. Em virtude da existência destas variáveis, determinar o nível exato de enzimas secretadas por um indivíduo normal é muito difícil.
Etiologias
As causas de IP em crianças podem ser divididas em 2 categorias:
– hereditárias
– adquiridas
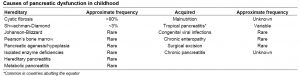
A maioria das causas hereditárias faz parte de doenças sistêmicas, como explicitado no quadro 1, abaixo.
Apresentação Clínica da Insuficiência Panceática
O diagnóstico é em grande essência clínico. No caso de um determinado paciente ser portador de alguma causa conhecida de IP que se apresenta com perda de peso e esteatorreia, está indicado o início do tratamento sem que seja necessária a realização de extensa investigação laboratorial. A IP se instala quando restar menos de 10% da função pancreática exócrina.
Esteatorreia (fezes espumantes, malcheirosas que boiam no vaso sanitário), perda de peso, desconforto e distensão abdominal são sintomas comuns relacionados com a digestão inadequada dos lipídios.
Inicialmente, a digestão de proteínas e amido se mantém adequada. Com a progressão da IP a má absorção de lipídios leva ao quadro de desnutrição, má absorção de vitaminas lipossolúveis (A, D, E, K), depleção de micronutrientes e diminuição de lipoproteínas circulantes.
A IP exócrina pode por si só, de forma isolada, causar ou exacerbar transtornos da motilidade do trato digestivo. Nestas circunstâncias, há alteração na regulação neuro-hormonal, especificamente na produção de colecisticinina e polipeptídeos pancreáticos (afetados pelo alimento não digerido no intestino), levando ao esvaziamento rápido do estômago e alterando a motilidade antroduodenal e da vesícula biliar.
Nos pacientes, nos quais o tratamento ainda não se iniciou, é notório o fato de que se alimentam em curtos espaços e que apresentam tempo de trânsito no intestino delgado mais rápido, cujos sintomas podem ser revertidos com o emprego de enzimas pancreáticos exógenos.
Diagnóstico
A caracterização diagnóstica pode ser estabelecida por métodos diretos e indiretos, a saber:
strong>Indiretos: são menos invasivos, mas que apresentam alta sensibilidade e especificidade, tais como:
– determinação quantitativa da eliminação de gordura nas fezes, as quais devem ser coletadas por um período de 72 horas, pelo método de Van de Kamer;
– elastase fecal, dosada pela técnica ELISA, e que avalia exclusivamente a produção enzimática endógena;
– quimiotripsina fecal, determinada por método colorimétrico, avalia a produção de ambas enzimas, endógenas e exógenas, portanto, pode apresentar resultados duvidosos em pacientes em vigência de terapia de reposição enzimática.
Diretos (quantitativos)
– teste da secretina-ceruleina;
– teste da secretina-pancreozimina (padrão-ouro, porém invasivo, sem valores de referência bem definidos em crianças).
- Teste da secretina-pancreozimina
Deve-se utilizar sonda gastroduodenal de dupla via posicionada sob controle fluoroscópico; uma das vias drena o conteúdo gástrico e a outra o duodenal. Secreções duodenais são coletadas em intervalos de 10 minutos, em três períodos após injeção intravenosa de secretina e em três períodos após infusão intravenosa de pancreozimina. Os aspirados são avaliados quanto ao volume, medida do pH, concentração de bicarbonato, amilase, tripsina, lipase, bilirrubinas, fosfatase alcalina, cálcio e magnésio. Amostras são encaminhadas para microscopia e citologia. A ocorrência de produção enzimática reduzida após injeção de pancreozimina corresponde ao índice mais sensível para avaliar a diminuição da função pancreática.
Principais Enfermidades Causadoras de Insuficiência Pancreática
Fibrose Cística
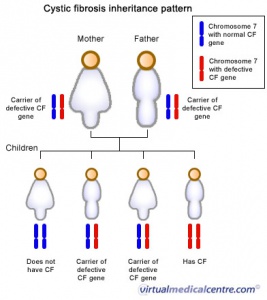
Trata-se de doença de herança autossômica recessiva que afeta múltiplos tecidos secretores epiteliais cuja incidência é de 1:3000 nascidos vivos em indivíduos caucasianos (Figura 3).
As manifestações clínicas da FC são reflexo de mutações no gene CFTR (cystic fibrosis transmembrane condutance regulator). Geralmente ocorrem 2 mutações (forma clássica) ou 1 mutação (forma não-clássica), sendo a mais frequente aquela que afeta o gene ΔF508. Estas mutações no gene CFTR resultam em transporte anormal de sódio e cloro. Em condições normais, o cloro intraluminal é trocado por bicarbonato, o que torna o ambiente alcalino, permitindo, desta forma, que altas concentrações de proteínas fiquem em seu estado solúvel. Em virtude da mutação no gene, o resultado é a presença de uma secreção viscosa e ácida, levando à obstrução ductal. Esta obstrução resulta em destruição tecidual por retenção de enzimas proteolíticas, fibrose, substituição gordurosa, formação de cistos e insuficiência pancreática exócrina.
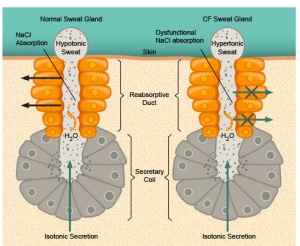
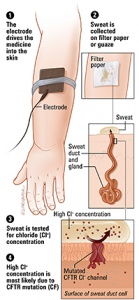
Figura 5- Esquema representativo comparando a glândula sudorípara de um indivíduo normal com a do portador de FC.
O mesmo ocorre com as secreções pulmonares (doença pulmonar crônica com infecções bacterianas recorrentes) e infertilidade no sexo masculino devido a azoospermia obstrutiva.
Nos recém-nascidos deve-se suspeitar do diagnóstico de FC na presença de íleo meconial, prolapso retal, “suor salgado”, icterícia prolongada, anemia hemolítica sem causa aparente, hipoalbuminemia e edema.
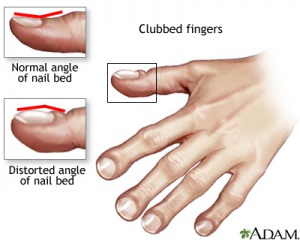
Nas crianças maiores a existência de dedos em baquetas de tambor, pólipos nasais, assim como secreção do trato respiratório colonizada por S. aureus ou P. aeruginosa, são achados importantes.
Triagem Neonatal
Desde 2001 o Ministério da Saúde criou o Programa Nacional de Triagem Neonatal, incluindo o diagnóstico precoce para FC, anemia falciforme e outras hemoglobinopatias.
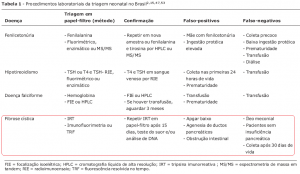
Realiza-se rotineiramente a dosagem sérica do tripsinogênio imunorreativo (IRT), indicador indireto da doença pois avalia a integridade da função pancreática (Tabela 1).
Caso a dosagem revele-se positiva (>70ng/ml), deve-se realizar nova dosagem após 15 dias, e se o teste permanecer positivo, deve-se realizar teste genético ou teste do suor.
O Íleo meconial pode estar relacionado a testes falso‐negativos, pois com a desobstrução intestinal ocorre rápida queda dos níveis de IRT no sangue. Mesmo diante de um IRT normal, o que não descarta completamente o diagnóstico de FC, se uma criança apresentar sintomas sugestivos da doença, deve ser submetida ao teste do suor.
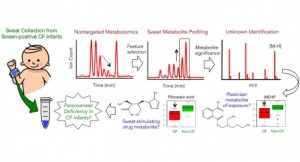
Figura 8- Representação esquemática das provas laboratoriais para a confirmação diagnóstica de FC desde o nascimento.
Diagnóstico
O diagnóstico de FC deve ser suspeitado na presença de uma ou mais manifestações fenotípicas (clínicas) características:
- Doença sinusal ou pulmonar crônica e/ou;
- Insuficiência exócrina pancreática crônica e/ou;
- História familiar de FC confirmada e/ou;
- Teste duplamente positivo de triagem neonatal.
Associada(s) à evidência de elevação anormal da concentração de Cloro no suor, em duas ocasiões diferentes ou, em casos especiais, deve-se solicitar a identificação genética de duas mutações da FC.
O teste do suor realizado pelo teste da iontoforese de pilocarpina é o método mais sensível para o diagnóstico da FC. As seguintes definições são recomendadas para a interpretação do teste do suor:
– concentração de Cloro >60 mmol/l dá suporte para o diagnóstico de FC;
– concentração intermediária de Cloro entre 40‐60 mmol/l é sugestivo, porém não diagnóstico;
– concentração de Cloro <40 mmol/l é normal;
– a concentração de Sódio não deve ser interpretada na ausência da respectiva dosagem do Cloro;
– condutividade <60mmol/l é improvável estar associada a FC e valores >90mmol/l são sugestivos de FC.
Tratamento da insuficiência pancreática exócrina
Recomenda-se a terapia de substituição enzimática, de acordo com cada caso (pancreolipase). A dose de enzimas baseia-se no peso do paciente e deve começar com 1000 unidades de lipase/kg/refeição para crianças com menos de 4 anos de idade, e com 500 unidades de lipase/kg/refeição para crianças com mais de 4 anos; a dose deve ser ajustada de acordo com a gravidade da doença, o controle da esteatorréia e a manutenção de um bom estado nutricional; de um modo geral, os pacientes não devem exceder a dose de 10.000 unidades de lipase/kg de peso por dia.
As enzimas pancreáticas exógenas devem ser ingeridas antes de cada refeição. A adequação da dose das enzimas ingeridas deve ser realizada através da dosagem da gordura fecal coletadas durante 72h (Van de Kamer), além da avaliação clínica levando-se em consideração a curva ponderal e a ocorrência ou não de diarreia.
A elastase fecal e a quimiotripsina fecal servem para avaliar a função pancreática, mas não para ajustar a dose de enzimas.
Colonopatia fibrosante:
Trata-se da complicação causada pelo uso crônico de altas doses de enzimas pancreáticas para o controle da má absorção. A dose de enzima associada a esta complicação varia de 24.000 UI a 50.000 UI de lipase/kg/dia. Como resultado, há deposição de colágeno na submucosa do intestino grosso, com consequente fibrose.
Fracasso no tratamento:
No caso de haver um fracasso terapêutico, como primeiro passo deve-se avaliar a aderência ao tratamento, à dieta e à hora de administração da enzima. A primeira opção é aumentar a dose de lipase oferecida e observar a resposta. Caso não houver sucesso, recomenda-se modificar a dieta, em particular reduzindo o consumo de gordura para 50 a 75 g/dia. Deve-se também reduzir o consumo de fibras, álcool, cálcio e magnésio, pois estas substâncias podem contribuir para aumentar a esteatorreia. Quando necessário o próximo passo é administrar medicamentos anti-ácidos, como inibidores do H2 ou inibidores da bomba de prótons. Caso não ocorra diminuição da esteatorreia, é recomendada a investigação de possível infestação por Giardia e, também, a existência de sobrecrescimento bacteriano no intestino delgado.
Síndrome Shwachman-Diamond (SSD)
Esta enfermidade foi descrita primeiramente em 1964 e, seguindo a FC, é a causa mais comum de insuficiência pancreática exócrina em crianças. Sua etiologia é desconhecida, porém, tudo indica ser de herança autossômica recessiva. A insuficiência pancreática apresenta gravidade variável e é um achado consistente da síndrome. A lesão pancreática é devida a uma falha do desenvolvimento acinar do pâncreas. Nesta síndrome ocorre um extenso remodelamento gorduroso do tecido do pâncreas com arquitetura ductular normal.
Mais de 98% da capacidade acinar exócrina do pâncreas deve estar comprometida para que os sintomas da insuficiência pancreática apareçam. Usualmente a esteatorréia surge nos 6 primeiros meses de vida em 50% dos casos, e em 90% antes de 1 ano de vida. Níveis baixos de tripsinogênio pancreático e isoamilase são marcadores úteis de insuficiência pancreática em pacientes com SSD. Em contraste com a FC, a função pancreática frequentemente melhora com a idade.
Excluir o diagnóstico de FC pelo teste do suor é essencial. O IRT na SSD deve ser normal ou baixo, pois também em contraste com a FC, a insuficiência pancreática é secundária à hipoplasia, não à obstrução/destruição do pâncreas.
A medida da elastase fecal é um bom método para triagem. A Tomografia Computadorizada, a Ressonância Magnética e a Ultrassonografia frequentemente mostram um pâncreas pequeno, com estrutura anormal e composto principalmente por gordura.
Hepatomegalia é encontrada em 15% dos casos e entre 50% e 75% deles apresentam enzimas de avaliação da função hepática em níveis de 2 a 3 vezes acima do valor da normalidade, isto se deve à esteatose hepática.
Além das manifestações de insuficiência pancreática também podem ocorrer inúmeras outras anormalidades extra-pancreáticas conforme as que estão descritas na Figura 12 e no Quadro 2, abaixo.
O Quadro 3 apresenta um esquema dos critérios diagnósticos da SSD.
A maioria dos pacientes requer suplementação de enzimas pancreáticas, entretanto, a esteatorreia desaparece espontaneamente em aproximadamente 50% dos casos.
A reposição de vitaminas lipossolúveis está indicada (A, D, E e K). O tempo de protrombina quando está anormal pode ser útil como marcador para deficiência de vitamina K.
Síndrome Johanson-Blizzard
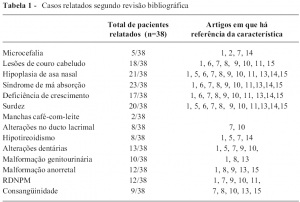
Trata-se de uma síndrome rara, multissistêmica de herança autossômica recessiva, decorrente de mutação no gene UBR1 no cromossomo 15q15-21, descrita pela primeira vez em 1971. Até 2002, tinham sido relatados 38 pacientes com esta síndrome, sendo a insuficiência pancreática um achado constante em 37 deles. Outros achados frequentes são: aplasia da aleta nasal, surdez, hipotireoidismo, ausência de dentes permanentes, aplasia do couro cabeludo e insuficiência pancreática exócrina (Tabela 1).
A agenesia da cartilagem nasal torna o diagnóstico da síndrome mais fácil, bem como a ausência de anomalias na medula óssea e esqueléticas a diferencia da SSD. A insuficiência pancreática é devida a defeitos primários das células acinares, similar ao que ocorre na SSD. A Tomografia Computadorizada do abdome mostra remodelamento gorduroso do pâncreas. Vale ressaltar que há descrição de evolução para insuficiência pancreática endócrina (Diabetes mellitus).
É importante enfatizar que nos lactentes a morte pode ocorrer em virtude de má absorção grave secundária ao quadro de insuficiência pancreática.
O tratamento é feito com reposição de enzimas pancreáticas.
Síndrome de Pearson
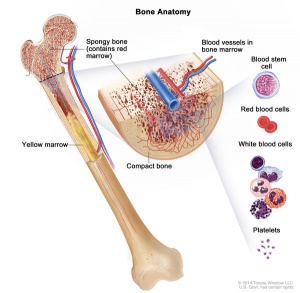
Trata-se de síndrome rara, caracterizada por insuficiência pancreática exócrina associada a anemia sideroblástica refratária ao tratamento. Logo após o nascimento, há anemia macrocítica com graus variáveis de neutropenia e trombocitopenia. O aspirado da medula óssea mostra vacuolização marcante dos precursores eritróides e mieloides, juntamente com grau intenso de sideroblastos em anel e hemossiderose, diferente dos achados descritos na SSD.
Os pacientes evoluem com déficit de crescimento e requerem transfusões sanguíneas frequentes. Os testes da função qualitativa pancreática revelam depressão da função acinar (análises de autópsias mostram atrofia das células acinares e fibrose).
O tratamento da disfunção pancreática também é realizado com reposição enzimática.
Conclusão
As causas de insuficiência pancreática podem ser de natureza variável e muito embora os casos de pancreatite aguda e/ou crônica sejam prevalentes na vida adulta, por outro lado, na infância as principais causas são de origem hereditária, e, portanto, devem chamar a atenção do clínico desde o período neonatal e ao longo do primeiro ano de vida. Deficiência do ganho pondero-estatural associada a diarreia com esteatorreia são as manifestações clínicas mais importantes e que devem levar a suspeição de insuficiência pancreática. Nestas circunstâncias impõem-se que a investigação diagnóstica seja realizada o mais rapidamente possível, visando proporcionar que o tratamento de reposição enzimática seja instituído de forma eficaz, para evitar a evolução para desnutrição e risco de vida.